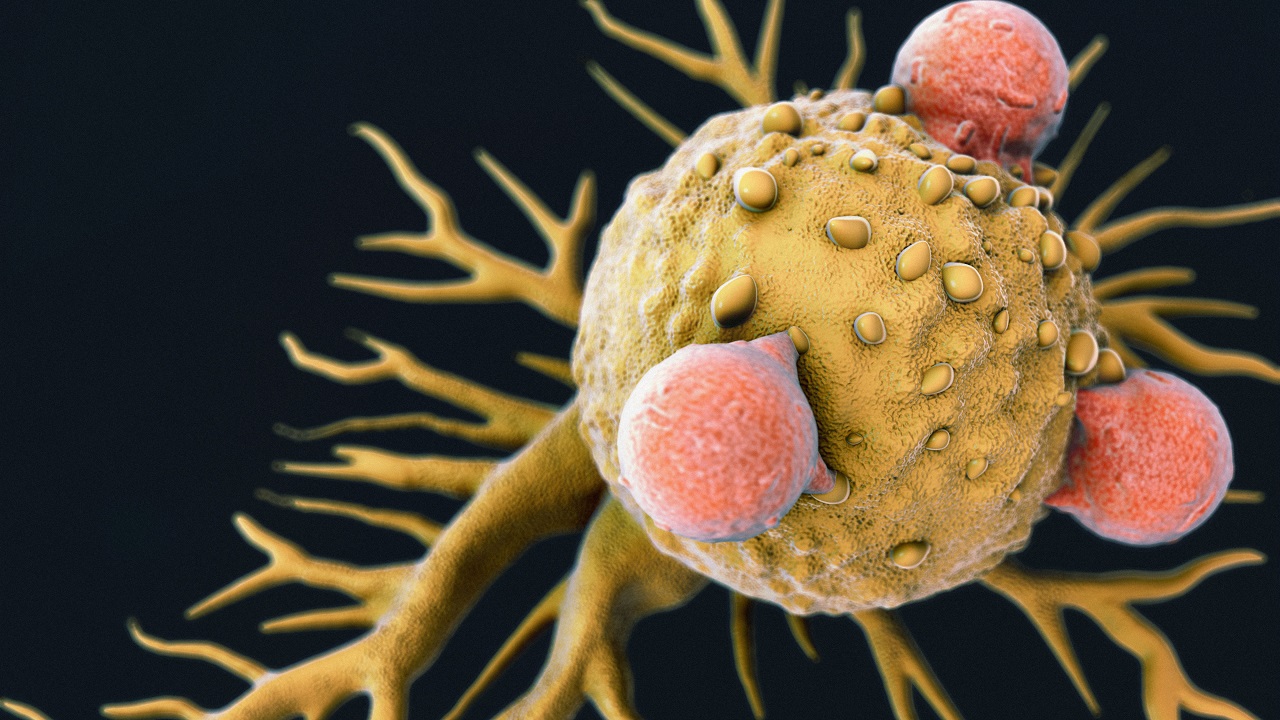
ჩვენი ფილტვები, ძვლები, სისხლძარღვები და სხვა ყველა ორგანო შედგება უჯრედებისგან; ერთ-ერთი გზა, რომლითაც ორგანიზმი ჯანმრთელობას ინარჩუნებს, არის ინფორმაციული ცილების, სახელად ლიგანდების გამოყენება; ეს ცილები უჯრედების ზედაპირზე არსებულ რეცეპტორებს ეკვრის და არეგულირებენ ბიოლოგიურ პროცესებს. როდესაც ეს ცილები მახინჯდება, შეიძლება გაგვიჩნდეს სხვადასხვა დაავადება.
ახლახან, მკვლევართა ჯგუფმა, რომელსაც სტენფორდის უნივერსიტეტის ბიოინჟინერიის დეპარტამენტის თავმჯდომარე ჯენიფერ კოჩრანი ხელმძღვანელობდა, ერთი ლიგანდი ოდნავ სხვადასხვა გზით დაამუშავა და ორი სრულიად სხვანაირი შედეგი მიიღო. ერთმა ცვლილებამ ნერვული უჯრედების აღდგენა გამოიწვია, ამავე ცილის სხვა ცვლილებამ კი ფილტვის სიმსივნის ზრდა ჩაახშო.
ექსპერიმენტები ადამიანის უჯრედებზე, ვირთაგვასა და თაგვებზე ჩატარდა, ნამდვილი დაავადებების თანხლებით, მაგრამ ჯერ შორსაა ადამიანებზე გამოცდისგან. თუმცა, შედეგები აჩვენებს, რამდენად მიუახლოვდნენ მკვლევრები სხეულის ცილაზე დაფუძნებული კონტროლის მექანიზმს, რომელიც სასიცოცხლო ორგანოებს თვითმკურნალობაში ეხმარება.
„ერთ მშვენიერ დღეს, ეს ცილები შეიძლება გამოვიყენოთ ნეიროდეგენერაციული დაავადების, სიმსივნეებისა და სხვა დარღვევების სამკურნალოდ, მათ შორის, ოსტეოპოროზის (ძვლოვანი ქსოვილის დავიწროება) და ათეროსკლეროზის შემთხვევებში“, — ამბობს კოჩრანი.
მის ლაბორატორიაში იკვლევენ, როგორ მუშაობენ ლიგანდები და რეცეპტორები უჯრედებთან შეტყობინებების მისატანად ერთობლივად და როგორ არის შესაძლებელი, რომ ასეთი ურთიერთქმედებები ინჟინერიის გზით შეიქმნას პოტენციური სამკურნალო აგენტების წარმოსაქმნელად. ფორმა კრიტიკული კონცეპტია. ყველა სხვა ცილის მსგავსად, ლიგანდები და რეცეპტორები შედგება მრავალი სხვადასხვა ამინომჟავისგან, რომლებიც მარგალიტების მსგავსად არის ჩალაგებული და ჩაკეცილია განსხვავებულ, სამგანზომილებიან ფორმებში. შესაბამისი ფორმის მქონე ლიგანდი დამთხვეულ რეცეპტორს ისე ერგება, როგორც გასაღები საკეტს.
დახვეწილი მოლეკულური ინჟინერიის მეთოდის გამოყენებით, მკვლევრებს შეუძლიათ ლიგანდში შეცვალონ აინომჟავების შემადგენლობა და დაამზადონ მილიონობით გასაღები და შემდეგ შეამოწმონ, რომლებს შეეძლებათ შესაბამისი რეცეპტორების გახსნა სასურველი გზით. გასაღებს, რომელიც უკეთ ერგება და უფრო საკეტისკენ უფრო ეფექტიანად მოგზაურობს, მეცნიერები სუპერაგონისტს უწოდებენ და მას შეუძლია უჯრედთან მიიტანოს შეტყობინება, რომელიც შეიცავს ინსტრუქციას უფრო მძლავრად ზრდის შესახებ. ბიოინჟინერიით შესაძლებელია ლიგანდების გადაქცევა ანტაგონისტებადაც — გასაღებებად, რომელიც ასევე ერგება რეცეპტორ საკეტს, მაგრამ ისე, რომ ბლოკავს სიგნალს და შესაბამისად, შეუძლია შეაფერხოს ისეთი ფუნქცია, როგორიცაა ზრდა.
შარშან, კალიფორნიის უნივერსიტეტის კიბოს მკვლევარ ალეხანდრო სვიტ-კორდეროსთან ერთად, კოჩრანმა გამოაქვეყნა კვლევა, რომელშიც ნაჩვენებია, როგორ მოახერხა რეცეპტორი ცილა CNTFR-ის ინჟინერიის გზით დამუშავებულმა ვერსიამ ფილტვის კიბოს ზრდის შეჩერება მღრღნელებში.
ამ კვლევაზე დაფუძნებული ახალ ექსპერიმენტში, მკვლევართა ჯგუფმა ჯუნ კიმის ხელმძღვანელობით, ინჟინერიით შექმნა ლიგანდი სახელად CLCF1, რომელიც რეცეპტორ CNTFR-ს ეკვრის. CLCF1-ში ამინომჟავების ერთი წყების გადაკეთების შედეგად, კიმმა ეს ლიგანდი სუპერაგონისტად გარდაქმნა. როდესაც ეს სუპერაგონისტი დაზიანებული ნერვული უჯრედების ქსოვილის კულტურას დაამატეს, ინჟინერიით შექმნილმა CLCF1-მა გაზარდა შეტყობინების შემცველი სიგნალები, რომლებმაც ხელი შეუწყო აქსონების, ანუ ნერვული იმპულსების გადამცემი ბოჭკოების ზრდას; ეს კი იმაზე მიუთითებს, რომ მოდიფიცირებული ლიგანდი დაზიანებულ ნეირონებს თავად აღდგენისკენ აგულიანებდა.
გარდა ამისა, კიმმა და მისმა კოლეგებმა შეძლეს საპირისპიროც — CLCF1-ის რამდენიმე დამატებითი ამინომჟავის შეცვლით, ეს ლიგანდი პოტენციურ ანტაგონისტად გარდაქმნეს, რომელმაც თაგვებში ფილტვის კიბოს ზრდა ჩაახშო, რაც ამ მოლეკულის ვარიანტის კიდევ ერთი სამედიცინო გამოყენების შესაძლებლობაზე მიუთითებს.
მთელი კარიერის განმავლობაში, კოჩრანი მუშაობს ინჟინერიის გზით ახალი ცილების შექმნაზე, რომლებიც პოტენციური სამკურნალო საშუალებებია ონკოლოგიაში და რეგენერაციულ მედიცინაში. მის ლაბორატორიაში აღმოჩენილი რამდენიმე მოლეკულა უკვე პრეკლინიკური განვითარების ბოლო ეტაპზეა; ადამიანებზე ცდებს კი უკვე გადის მის მიერ ამ გზით შექმნილი საკვერცხეებისა და თირკმლის კიბოს სამკურნალო საშუალება. კოჩრანი იმედიანად არის განწყობილი და სჯერა, რომ ინჟინერიით შექმნილი ლიგანდები და რეცეპტორები დაამტკიცებს, რომ პრეპარატების იმედისმომცემი კლასია დაავადებებთან საბრძოლველად.
კვლევა ჟურნალ PNAS-ში გამოქვეყნდა.
მომზადებულია stanford.edu-ს მიხედვით.